 Дефицитная адгезия лейкоцитов -
это заболевание иммунной системы, передающееся по наследству. Тяжесть болезни
заключается в неспособности лейкоцитов противостоять любой инфекции. По сути,
лейкоциты являются главным защитником организма человека с разными
заболеваниями. Они, имея специальные
ферменты, просто «переваривают» вирусы и микроорганизмы, расщепляют опасные
белковые вещества. К тому же, освобождают кровь от продуктов распада,
образующихся в результате жизнедеятельности органов. Лейкоциты - это бесцветные
кровяные клетки, размером до 20 микрон, неправильной (или округлой) формы. Ещё
они называются – белые кровяные тельца.
Дефицитная адгезия лейкоцитов -
это заболевание иммунной системы, передающееся по наследству. Тяжесть болезни
заключается в неспособности лейкоцитов противостоять любой инфекции. По сути,
лейкоциты являются главным защитником организма человека с разными
заболеваниями. Они, имея специальные
ферменты, просто «переваривают» вирусы и микроорганизмы, расщепляют опасные
белковые вещества. К тому же, освобождают кровь от продуктов распада,
образующихся в результате жизнедеятельности органов. Лейкоциты - это бесцветные
кровяные клетки, размером до 20 микрон, неправильной (или округлой) формы. Ещё
они называются – белые кровяные тельца.
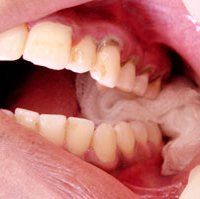
Симптомы недостатка лейкоцитарной
адгезии выявляют по следующим признакам: частые бактериальные инфекции, тяжёлые
гингивиты, отсутствие должного количество гноя при воспалении медленно
заживающих ран. И это основные свидетельства нарушений системы иммунитета.
Клиника заболевания проявляется
грибковыми и бактериальными рецидивирующими инфекциями: слизистой рта и половых
органов, кожи, кишечника, лёгких. Лейкоцитоз становится стойким и достигает 15-20 тыс. на 1/мкл; инфекции на коже осложняются некрозами с быстрым увеличением
очага поражения. После медленного заживления остаются сформированные уродливые
рубцы.
Причина заболевания
Если рассматривать основные и
общие факторы, то причина кроется в мутациях, которые нарушают функционирование
поверхностного белка адгезии бета-интегрина. При иммунной реакции клеток на
появление инфекции этот белок играет главную роль. Если же он слаб,
неполноценен, то процесс противостояния нарушается и работа лейкоцитов при
защите организма от инфекционного поражения или воспалительной реакции
становится неэффективной и ослабленной.
В большинстве причин этого заболевания называют наследственность.
Исследованы два наследственных вида отклонений дефицита лейкоцитной адгезии.
Оба передаются аутосомно-рецессивно и приводят к дистрофии нейтрофилов, то есть
- слабость для выхода из кровеносного русла в направлении очага инфекции. В
итоге формируется устойчивый лейкоцитоз и лёгкая восприимчивость к инфекциям.
Причиной «первого» типа недостаточной адгезии лейкоцитов является мутация
гена, курирующего CD18, общую для бета 2-интегринов совместную субъединицу.
В результате нарушается плотность
адгезии нейтрофилов к эндотелиальным клеткам. Клиника заболевания протекает в
зависимости от агрессивности мутантного гена. В наихудшем случае молекул
адгезии в лейкоцитах нет и совсем нет на неактивированных нейтрофилах. И под
влиянием «провоспалительных цитокинов» молекулы не могут выходить ни на
активированные Т- и В-лимфоциты, ни на нейтрофилы. Хорошо изучены
функциональные нарушения нормальных свойств лейкоцитов, так как важность
молекул адгезии для лейкоцитов просто бесценна. Нейтрофилы и моноциты теряют
способность «приклеиваться» к эндотелиальным клеткам и белковой поверхности, а
также теряются свойства «распластывания», агрегации и хемотаксиса.
Причиной «второго типа»
недостаточной адгезии лейкоцитов иногда являются основные возбудители
стафилококус айрес и энтеробактерии. Синдром дефицита лейкоцитной адгезии «типа
2» объясняется дефектом CD 15 – антигена сиалированного Lex. Этот
поверхностный гликопротеид является лигандом для селектинов эндотелиальных
клеток.
Диагностика заболевания для обоих типов
Недостаточность лейкоцитарной
адгезии (Leukocyte Adhesion Deficiency, LAD-1) «первого» типа: предполагается
при изучении родственных связей и семейных заболеваний. Здесь ведущее место
занимает наследственность. Заболевание зафиксировано у лиц обоего пола без
особых различий. Диагносцирование подтверждает мутацию гена, кодирующего
бета2-субъединицу интегрина нейтрофилов. Количество на поверхности клеток
рецепторов, влияющих на процессы адгезии (CD11a/CD18) довольно снижены и точно
не определяются. LAD-1 характеризуется отдельными нарушениями
трансэндотелиальной адгезии и хемотаксиса нейтрофилов, а также возможностью «переваривать»
СЗ-опсонизированные бактерии. Диагностику недостатка адгезии лейкоцитов «первого
типа» осуществляют на основании иммунофенотипирования нейтрофилов. Для этого
широко применяется метод «проточной цитометрии». Он показывает степень недостающей
экспрессии CD18 и CD11а на нетрофильной поверхности.
В целом, картина заболевания LAD
зависит от степени выраженности дефекта. В организме пациентов с явным
отсутствием СД18/СД11а начало заболевания легко замечается, а потом явно
наблюдается. Иногда его можно определить даже в первые недели после рождения:
незаживающая пупочная рана, периректальный целлюлит, язвенные стоматиты, омфалит и сепсис с
фатальным развитием. При средней умеренной выраженности дефекта – это наличие
частых бактериальных инфекций. Поражают они прежде всего кожно-слизистые области,
затем, поражения ЖКТ – гастрит, эзофагит, энтероколит. Имели место и случаи периодонтитов, синуситов. Нередко в очагах воспаления почти не бывает гноя. В
разгар активной инфекции типичный персистирующий лейкоцитоз (иногда и
гиперлейкоцитоз), а также и нейтрофилёз снижает нейтрофильное число. Но при
условии реконвалесценции.
Недостаточность адгезии лейкоцитов
(Sialyl-Lewis X, LAD-2) «второго» типа:
«Обусловленный» структурный дефект. Наиболее вероятный тип, также по
наследованию. Он так же как и первый тип, считается аутосомно-рецессивным, но
встречается крайне редко. Адгезию нейтрофилов LAD-2 чаще всего связывают с
нарушенным циклом метаболизма фукозы, и
следовательно с произошедшей мутации фукозилтрансферазных генов. Клиническая
картина и принципы терапевтического лечения LAD-2 аналогичны лечению, как и при
LAD-1. Сбой фукозилирования, присущий для LAD-2, кроме «обязательного»
иммунодефицита, ещё проявляется в специфическом генотипе больных, особенно у детей.
Это - плоское лицо, широкие ладони, широкая переносица, маленький рост,
короткие конечности, а самое печальное - отставание в умственном и психическом
развитии. У этих больных, нейтрофилы не могут и не способны «приставать» к
эндотелию сосудов. Поэтому нет возможности проникнуть в очаг воспаления и
локализовать его.
Другие нехарактерные аномалии,
схожие с недостаточной подвижностью нейтрофилов, также исследованы и описаны,
но в единичных случаях.
Чаще стали применять генетические
тестирования. Принцип тестирования основан на использовании новейших молекулярных
и генетических знаний, с применением современных технологий. Тестирование можно
проводить в любом возрасте. По результатам процесса тестирования анализируется
мутация в ДНК, ведущая к развитию данной болезни. В итоге выявляется дефектная
(мутантная) копия гена и нормальная копия гена.
Лечение
Лечение недостаточности адгезии
лейкоцитов в обоих случаях (типах), заключается в правильности выбора
антибактериального лечения. Особенно, в перспективе на период обязательных
сезонных инфекций, учитывая все результаты бактериологических анализов. При
неожиданных обострениях заболевания, хорошо иметь возможность купирования
инфекции, включая трансфузии гранулоцитов. Поставленный
диагноз неутешительный. Прогнозы крайне неблагоприятные. Эффективное
излечение полностью, возможно лишь при проведении аллогенной
трансплантации костного мозга. А для этого необходимо иметь идеально совместимого донора. В случае среднетяжёлого течения болезни, существенно помогает адекватная лекарственная (ко-тримоксазол)
и стоматологическая профилактика заболевания. Зарегистрированы факты
значительного снижения частоты и тяжести инфекций при неукоснительном
выполнении предписанных лечебных процедур и мероприятий.



Отзывы